چهارشنبه, ۱۲ اردیبهشت, ۱۴۰۳ / 1 May, 2024
مجله ویستا
تالاسمی، قفلی که کلیدی ندارد!
گوهر بخش سرشتین وجود آدمیزاد است که در واقع همان ژنتیک است که با فرد از مادر میزاید و هنر، آن پاره از وجود است که در طول زندگانی بعد از زادن در او شکل میگیرد.
آنان اعتقاد داشتهاند که تغییر گوهر، محال است و قفل یزدان به شمار میآید که بر آن کلیدی نیست. اکنون با این مقدمه در نشستی اجمالی به بررسی یک بیماری ژنتیک به نام تالاسمی میپردازیم. کلمه تالاسمی از واژه یونانی (تالاسا) به معنی دریا گرفته شده است و در مناطقی که مالاریا شایـع بوده، این انـگل منجر به نوعی جهش در افراد شده بهطوریکه مالاریا قادر به رشد در سلولهای خونی آنها نبوده و در نتیجه این افراد به انگل مالاریا مقاوم شده و زنده میماندند.
این بیماری به جز کشورهای اروپایی و آمریکایی در بیشتر نقاط دنیا گسترده است و بیشترین گستردگی در کشورهای مدیترانهای خاورمیانه، هندوستان، آفریقا، چین و آسیای جنوبشرقی است.
● عوامل بروز تالاسمی
عامل ابتلاء به این بیماری وراثت است. افراد مبتلا به این بیماری ژنهای معیوب را از والدین دریافـت میکنند که در نتیجه هموگلوبین تولید ناکافی خواهد داشت. هموگلوبین مولکول اصلی داخل گویچههای قرمز است که از هم (Heme ) و زنجیرههای پروتئینی یا گلوبین تشکیل شده است. در هر زنجیره گلوبین یک مولکول هم وجود دارد که اکسیژن را توسط آهن خود حمل میکند. پس تولید هموگلوبین نیاز به تامین آهن و ساخت هموگلوبین دارد. بهطور کلی ۴نوع هموگلوبین داریم که همه آنها شامل ۴ زنجیره پروتئینی هستند که در تمام انواع هموگلوبینها تعداد دو زنجیره آلفا یکسان است و تفاوت آنها در زنجیرههای بتا، گاما و دلتا است.
برای ساخت زنجیره بتا هر فرد از هر والد خود (پدر و مادر) یک ژن سازنده این زنجیره را دریافت میکند و برای زنجیرههای آلفا و دلتا از هر والد ۲ ژن دریافت میکند و براساس جهش یا حذف هر کدام از این ژنها ساخت و زنجیره مربوطه مختل شده و در واقع بهعلت اشکال در ساخت زنجیرههای پروتئینی هموگلوبین انواع بیماری تالاسمی را خواهیم داشت.
هموگلوبین نه تنها برای حمل و تحویل طبیعی اکسیژن لازم است بلکه در شکل و اندازه و بدشکلی گلبول قرمز دخالت دارد. مقدار کل هموگلوبین خون بهطور طبیعی در خانمها ۲±۱۲ و در آقایان ۲±۱۴ گرم در دسیلیتر است.
● انواع تالاسمی
تالاسمی به دو نوع آلفا تالاسمی و بتا تالاسمی تقسیم میشود که خود بتا تالاسمی هم شامل تالاسمی ماژور (تالاسمی شدید) و تالاسمی مینور یا تالاسمی خفیف است.
▪ تالاسمی مینور
تالاسمی مینور معمولا بدون علامـت بوده و علایم بالینی واضـح ندارند و بهطور عمده در تستهای چکاپ بهصورت اتفاقی تشخیص داده میشوند. این افراد کم خونی مختصری دارند که معمولا مشکلساز نیست. تالاسمی مینور در نتیجه اختلال یکی از دو ژن سازنده زنجیره بتا به وجود میآید که این ژن ناقص یا از پدر و یا از مادر به فرد به ارث رسیده است.
نکتهای که در تالاسمی مینورنوع بتا جالب توجه است، این است که این افراد نباید با یک فرد شبیه خود (تالاسمی مینور) ازدواج کنند. اگر دوفرد تالاسمی مینورباهم ازدواج کنند به احتمال ۲۵درصد فرزندشان دچار تالاسمی شدید (ماژور) خواهد بود و ۲۵درصد فرزندانشان سالم و ۵۰درصد تالاسمی مینور خواهند داشت.
▪ تالاسمی ماژور
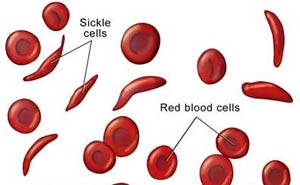
تالاسمی ماژور معمولاً طی چند ماه اول تولد تشخیص داده نمیشود. تالاسمی ماژور یا آنمی کولی بهعلت حذف یا جهش در هر دو ژن سازنده زنجیره بتا ایجاد میشود و به این ترتیب یا هیچ زنجیره بتایی ساخته نمیشود یا به مقدار کمی ساخته میشود. در نتیجه بدن کمبود این زنجیرهها را با ساخت زنجیرههای آلفا جبران میکند که این زنجیرههای آلفای اضافی برای گلبولهای قرمز سمی هستند و با رسوب روی سلولهای گلبول قرمز باعث میشوند که گلبولهای قرمز در مغز استخوان و در داخل خون تخریب شده و زنجیرههای آلفا در مغز استخوان رسوب کنند.
از طرفی بهعلت خونسازی غیرمؤثر، مراکز خونساز خارج مغز استخوان، ازجمله کبد و طحال شروع به خونسازی میکنند و بزرگ میشوند. بیماری معمولا بهصورت کمخونی شدید در ۶ ماهه اول زندگی کودک تظاهر میکند و درصورت عدمشروع تزریق خون، بافت مغز استخوان و مکانهای خونساز خارج مغز استخوان فعال و بزرگ شده و باعث بزرگی مغز استخوانها بهخصوص استخوانهای پهن (صورت و جمجمه) و بزرگی کبد و طحال میشوند.
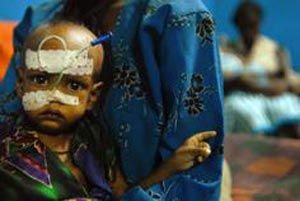
● علائم بیماری
افزایش حجم شدید مغز استخوان بهخصوص در استخوانهای صورت و جمجمه، چهره خاصی را برای افرادی که تالاسمی دارند ایجاد میکند (چهره موش خرمایی.)
کم خونی شدید طوری که برای بقاء بیمار تزریق مکرر خون لازم است.
- اختلال رشد دربچههای بزرگتر
- رنگ پریدگی، زردی و گاهی پوست ممکن است بهدلیل رنگ پریدگی و یرقان و رسوب رنگدانه به رنگ مس در آید.
- بزرگی کبد و طحال: در سنین بالاتر گاهی طحال به حدی بزرگ میشود که باعث تخریب بیشتر گلبولهای قرمز میشود.
- علایم ناشی از رسوب آهن در بافتهای مختلف از جمله پانکراس و قلب و غدد جنسی و ایجاد دیابت و نارسایی قلبی و تاخیر در بلوغ.
- استخوانها نازک شده و مستعد شکستگی میشوند.
● تشخیص تالاسمی قبل از تولد
امروزه تشخیص سندرمهای تالاسمی بااستفاده از DNA و بر پایه PCR ( بررسی ژنها) در دوران قبل از تولد امکان پذیر است. DNA جنین از طریق آمینوسنتز (کشیدن مایع آمینوتیک یا کیسه آب) یا نمونه برداری از پرزهای جفتی به دست میآید که از این طریق ۹۰ تا ۹۵درصد امکان تشخیص امکانپذیر است.
▪ چگونه میتوان مانع تولد یک کودک مبتلا به تالاسمی شد ؟
بیماری تالاسمی از اولین ردههای پیشتاز بیماریهای ارثی در کشور ماست که باید کنترل شود، اگر چه بهترین روش پیشگیری، براندازی و کنترل تالاسمی از راه اکولوژیک شناخته شده ولی بهطور کلی چند روش پیشنهاد میشود:
ـ روش اول: خروج و دفع جنین مبتلا به تالاسمی از شکم مادر، قبل از پیدا کردن موجودیت انسانی است. با مشاوره ژنتیک در ازدواجهای دو شخص مینور با هم و نمونهبرداری از جفت (هفته ۱۲-۱۰ حاملگی) و بررسی DNA درصورتی که تشخیص داده شود که جنین مبتلا به تالاسمی ماژور است سقط صورت خواهد گرفت که اجازه شرعی آن نیز گرفته شده است.
ـ روش دوم: شناسایی ناقلین و ازدواج یک فرد سالم با ناقل که این روش باعث افزایش ناقلین در سطح جامعه در آینده میشود. روش سوم: کاهش موالید از طریق تنظیم خانواده که قادر به ریشهکنی واقعی نیست ولی از درجه ابتلا در جامعه میکاهد.
● درمان
تالاسمی ماژور را یا نباید درمان کرد و یا اگر درمان میکنیم خوب درمان کنیم چون اگر درمان به خوبی انجام شود بیماران میتوانند از نظر فیزیکی، تحصیلات، طول عمر عین افراد سالم باشند. ولی اگر بد درمان شوند بیمار دچار عوارض بیماری (تغییر قیافه، نارسایی کبد، قلب، کاهش رشد و اختلالات روانی و...) شده و عمر کوتاه همراه با زجر و صرف هزینه بالا خواهد داشت، در حالی که اگر درمان نشوند لااقل این زمان کوتاهتر خواهد بود. البته امیدواریم که اولاً با پیشگیریهای لازم کودک مبتلا به تالاسمی متولد نشود و یا اگر شد به بهترین وجه درمان شود و اما درمان قطعی تالاسمی ماژور پیوند مغز استخوان است که بهتریندهنده ابتدا خواهر و برادر و بعد پدر و مادر و در نهایت افراد دیگر است که با آزمایشهای اختصاصی تعیین میشود.
تالاسمی شدید و درمان نشده همیشه باعث مرگ در دوران کودکی میشود. درصورت تزریق مکرر خون و حفظ سطح مناسبی از خون میتوان طول عمر را افزایش داد و تا حد زیادی مانع از تغییرات استخوانی و اختلال رشد شد. اما دیگر راههای درمان تالاسمی عبارتند از:
▪ تزریق دراز مدت خون:
هدف از تزریق خون مکرر برای بیمار حفظ هموگلوبین بیمار در سطح بالای ۱۰ است.
▪ دفروکسامین:
مشکل اصلی بیماران تالاسمی بعد از سالها، رسوب آهن در بافتها و اضافه بار آهن است که میتوان آن را به کمک تزریق مرتب دفروکسامین بهصورت زیر جلدی یا وریدی تخفیف داد. این دارو با آهن ترکیب شده و از ادرار دفع میشود. البته مقدار زیاد این دارو ممکن است باعث واکنش پوستی در محل تزریق و یا عوارض عصبی به ویژه در دستگاه بینایی و شنوایی شود. بنابراین این دارو به تنهایی برای پیشگیری دراز مدت از مسمومیت با آهن کافی نیست.
▪ برداشتن طحال:
اگر بزرگی طحال، نیاز به تزریق خون را بیشتر کند طحال برداشته میشود تا نیاز به خون کاهش یابد.
قابل ذکر است بانک خون بند ناف نیز از راههای نوین درمان بیماریهای ژنتیک میتواند باشد. بانک خون بند ناف فرایندی است که خون خارج شده از بند ناف و جفت نوزاد شما بعد از تولد برای استفادههای پزشکی آینده جمعآوری، منجمد و ذخیره میشود. فرایند جمع آوری خون بند ناف برای نوزاد شما بدون درد و بیخطر است و مانع برنامههای شما برای تولد یا تصمیمات همسر شما برای قطع بند ناف نمیشود.
قابل ذکر است خون بند ناف بهطور موفقیت آمیزی در درمان لوسمی، نقص سیستم ایمنی، کمخونی داسی شکل و آنمی آپلاستیک، تالاسمی، لمفومها مثل بیماری هوچکین و شبیه آنها اما با شرایط شناخته شده کمتر استفاده شده است. اکثریت این بیماران سلولهای بنیادی بند ناف را از یک همنژاد یا غیرخویشاوند دریافت میکنند. امروزه تنها تعداد کمی از کودکان بهطور موفقیتآمیزی با خون بند ناف خودشان درمان میشوند زیرا همه این بیماریها پایه و اساس ژنتیک دارند.
بهعنوان مثال اگر یک بچه با بیماری لوسمی با خون بند ناف خودش درمان شده باشد بیماری او دوباره میتواند عود کند زیرا خون بند ناف او حاوی رمز ژنتیک برای لوسمی است. محققین در حال تحقیق راههایی برای اصلاح این موضوع هستند. تحقیقات امیدبخش جدید نشان میدهند که خون بند ناف ممکن است برای درمان افراد با شرایط گوناگونی مثل دیابت، آسیبهای طناب نخاعی، نارسایی قلبی، سکته و اختلالات نوروژنیک مثل مالتیپل اسکلروزیس استفاده شود. دانشمندان امیدوار هستند که روزی بیماران بزرگسال قادر باشند بهطور روزمره خون بند ناف خود را برای درمان دریافت کنند. محققان روشهای توسعه ظرفیت سلولهای بنیادی در یک واحد خون بند ناف را گسترش دادهاند و اکنون آنها را در آزمایشهای کلینیکی آزمایش میکنند. اما این فرایندها هنوز معمول و رایج نیستند.
● روند بیماری
امروزه با توجه به درمانهای موجود، بیماران تا ۳۰ سالگی هم زنده میمانند و اینها بچههایی با رشد ناقص هستند و شایعترین علت مرگ آنها نارسایی قلبی بهعلت رسوب آهن در بافتها و همچنین بهعلت تزریق خون و افزایش بار قلب است.
به امید آن روز که با رایزنیهای مناسب و آموزش و سرمایهگذاری در سطح کلان کشوری دیگر شاهد زجر کشیدن بیماران تالاسمی نباشیم.
پگاه سرامی
منبع : روزنامه همشهری
همچنین مشاهده کنید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید بلیط هواپیما
ایران مجلس شورای اسلامی بابک زنجانی مجلس چین دولت سیزدهم خلیج فارس دولت لایحه بودجه 1403 شورای نگهبان حجاب مجلس یازدهم
روز معلم تهران سیل قوه قضاییه آموزش و پرورش شهرداری تهران فضای مجازی پلیس سلامت دستگیری شورای شهر تهران سازمان هواشناسی
بانک مرکزی خودرو دلار قیمت دلار قیمت طلا قیمت خودرو ایران خودرو سایپا بازار خودرو مالیات تورم ارز
تلویزیون سریال سعید آقاخانی سینمای ایران سینما نون خ موسیقی تئاتر دفاع مقدس فیلم کتاب رسانه ملی
رژیم صهیونیستی اسرائیل غزه فلسطین آمریکا جنگ غزه حماس نوار غزه روسیه عربستان ترکیه افغانستان
فوتبال پرسپولیس استقلال رئال مادرید سپاهان تراکتور بایرن مونیخ باشگاه استقلال لیگ برتر فوتسال تیم ملی فوتسال ایران بازی
هوش مصنوعی اینستاگرام ناسا تبلیغات تسلا اپل فناوری گوگل همراه اول آیفون ماه
داروخانه کاهش وزن خواب مسمومیت دیابت طول عمر سلامت روان بارداری آلزایمر