سه شنبه, ۱۱ اردیبهشت, ۱۴۰۳ / 30 April, 2024
مجله ویستا
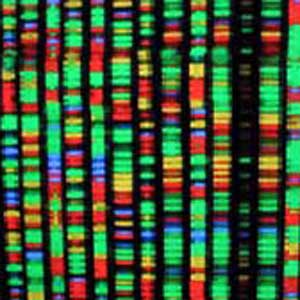
تنوع ژنتیکی و سلامت شخصی تا چه اندازه به هم مربوط اند؟

جنیفر كوزین
ترجمه:ع.فخر یاسری
منبع : روزنامه شرق
همچنین مشاهده کنید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید میز و صندلی اداری
خرید بلیط هواپیما
گیت کنترل تردد
ایران خلیج فارس حجاب مجلس شورای اسلامی مجلس روز معلم شورای نگهبان بودجه دولت سیزدهم جمهوری اسلامی ایران مجلس یازدهم قالیباف
پایتخت تهران سلامت شهرداری تهران هواشناسی فضای مجازی شورای شهر شورای شهر تهران سیل قتل پلیس وزارت بهداشت
خودرو ارز دولت قیمت دلار ایران خودرو قیمت خودرو مالیات دلار بازار خودرو بانک مرکزی قیمت طلا مسکن
تلویزیون مهران مدیری سریال رسانه سینمای ایران تئاتر فیلم موسیقی سینما سریال پایتخت کتاب
سازمان سنجش انتخاب رشته
غزه جنگ غزه فلسطین آمریکا حماس عربستان روسیه نوار غزه اوکراین ترکیه عراق طوفان الاقصی
فوتبال استقلال پرسپولیس سپاهان تیم ملی فوتسال ایران تراکتور فوتسال بازی وحید شمسایی باشگاه استقلال باشگاه پرسپولیس لیگ برتر
هوش مصنوعی اپل اینستاگرام همراه اول تبلیغات گوگل ایرانسل فناوری روزنامه آیفون
مواد غذایی ویتامین سازمان غذا و دارو طول عمر سلامت روان بارداری پرستار دندانپزشکی هندوانه