شنبه, ۸ اردیبهشت, ۱۴۰۳ / 27 April, 2024
مجله ویستا
دیمیتری اوانوویچ مندلیف

● ورود به دنیای شیمی
وی در سال ۱۸۶۹ دکتر علوم و استاد شیمی دانشگاه شد و در همین سال ازدواج کرد. در این هنگام ، فقط ۶۳ عنصر از نظر شیمیدانها شناخته شده بود.
● قانون تناوبی
مندلیف در این فکر بود که خواص فیزیکی و شیمیایی عناصر ، تابعی از جرم اتمی آنهاست. بدون قانون تناوبی نه پیش بینی خواص عناصر ناشناخته میسر بود و نه به فقدان یا غیبت برخی از عناصر میشد پی برد. کشف عناصر ، منوط به مشاهده و بررسی بود. بنابراین تنها یاری بخت ، مداومت و یا پیش داوری ، منجر به کشف عناصر جدید میشد.
قانون تناوبی ، راه جدیدی در این زمینه گشود. منظور مندلیف از این جملهها آن بود که در سیر تاریخی شیمیایی ، زمان حدس زدن وجود عناصر و پیشگویی خواص مهمشان فرا رسیده است. جدول تناوبی ، پایه ای برای این کار شد. حتی ساخت این جدول نشان میداد که در چه جاهایی مکان خالی باقی میماند که باید بعدا” اشغال شود.
● چینش عناصر در جدول تناوبی
با آگاهی از خواص عناصر موجود در جوار این مکانهای خالی ، میشد خواص مهم عناصر ناشناس را تخمین زد و چند مشخصه مقداری آنها (جرمهای اتمی، چگالی ، نقطه ذوب ، و نقطه جوش و مانند آنها) را به کمک نتیجه گیریهای منطقی و چند محاسبه ریاضی ساده ، تعیین کرد. این مطالب نیاز به تبحر کافی در شیمی داشت. مندلیف از این تبحر برخوردار بود که با ترکیب آن ، با تلاش علمی و اعتقاد به قانون تناوبی توانست پیشگوهای درخشانی درباره وجود و خواص چندین عنصر جدید را ارایه دهد. بنابراین مطابق با این فکر ، جدولی درست کرد و ۶۳ عنصر شناخته شده را به ترتیب جرم اتمیشان در جدول قرار داد.
تعداد عناصر در سطرهای جدول یکی نبود، مثلاٌ سطر پنجم ۳۲ عنصر داشت، در حالیکه سطر ششم فقط شامل ۶ عنصر بود. ولی عناصری که خواص آنها شبیه هم بود، در این جدول نزدیک هم قرار داشتند و بدین علت مقداری از خانههای خالی ، متعلق به عناصری است که تا آن زمان شاخته نشده بود. وی این نتیجه را در سال ۱۸۶۹ به جامعه شیمی روسیه تقدیم کرد.
● میزان استقبال از جدول مندلیف در آن زمان
جدول مندلیف که پیش بینی وجود ۹۲ عنصر را مینمود، جز “لوتر مایز” که یک سال بعد از مندلیف ، جدولی مشابه با جدول مندلیف انتشار داده بود، طرفداری نداشت.
▪ پیشبینیهای مندلیف در جهان علم
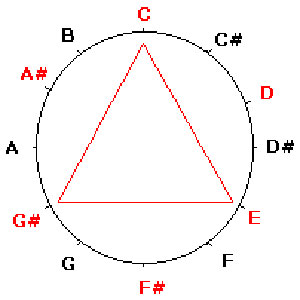
پیشبینیهای عجیب مندلیف ، زمان درازی به صورت مثلهای موجود در همه کتابهای شیمی در آمده بود و کمتر کتاب شیمی وجود دارد که در آن ، از اکاآلومینیوم و اکابور و اکاسیلیسیم یاد نشده باشد که بعدها پس از کشف به نامهای گالیوم، سکاندیوم و ژرمانیوم نامیده شدند. در میان سه عنصری که مندلیف پیش بینی کرده بود اکاسیلیسیوم بعد از سایرین کشف شد(۱۸۸۷) و کشف آن بیش از کشف دو عنصر دیگر ، مرهون یاری بخت و تصادف مساعد بود.
▪ تایید پیشگوییهای مندلیف
در واقع ، کشف گالیوم توسط “بوابودران” (۱۸۷۵) مستقیماٌ توسط روشهای طیف سنجیاش بود و جداکردن سکاندیوم توسط “نیلسون” و “کلو” (۱۸۷۹) مربوط به بررسی دقیق خاکهای نادر بود که در آن زمان اوج گرفته بود. اندک اندک همه پیشگوییهای مندلیف تحقق یافتند. آخرین تایید در مورد وزن مخصوص سکاندیوم فلزی بود.
در سال ۱۹۳۷ ، “فیشر” شیمیدان آلمانی ، موق به تهیه سکاندیوم با درجه خلوص ۹۸% شد. وزن مخصوص آن ، ۳ گرم بر سانتیمتر مکعب بود. این دقیقاٌ همان رقمی است که مندلیف پیشبینی کرده بود. در پاییز سال ۱۸۷۹ “انگلس” کتاب جامعی بدست آورد که نویسندگانش “روسکو” و “شورلمر” بودند. در آن کتاب ، برای نخستین بار به پیشگویی آلومینیوم توسط مندلیف و کشفش تحت تاثیر نام گالیوم اشاره شده بود.
در مقاله ای که بعدها انگلس در کتابی هم نقل کرده است، اشاره به مطلب آن کتاب شیمی شده است و نتیجه گرفته است که: « مندلیف با به کار بردن ناخودآگاه قانون تبدیل کمیت به کیفیت هگل ، واقیعت علمی را تحقق بخشید که از نظر تهور ، فقط قابل قیاس با کار “لوریه” در محاسبه مدار سیاره ناشناخته نپتون بوده است. »
● شهرت جهانی مندلیف
علاوه بر آنچه گفته شد، با اکتشاف آرگون در سال ۱۸۹۴ و هلیوم و اینکه جدول مندلیف وجود نیون و کریپتون و گزنون را پیشبینی نمود، جدول مندلیف شهرت عجیب و فوقالعاده ای کسب نمود. در آن سالها بود که تمامی آکادمیهای کشورهای جهان (غیر از مملکت خویش) او را به عضویت دعوت نمودند.
● مرگ مندلیف
مندلیف دو دوم فوریه ۱۹۰۷ در ۷۳ سالگی در گذشت. به طوری که میدانیم، از هنگامی که جدول مندلیف بوجود آمد، خانههای خالی آن ، یکی پس از دیگری با کشف عناصر پر میشد و آخرین خانه خالی جدول ، در سال ۱۹۳۸ با کشف آکتنیوم در پاریس پر شد.
منبع : دانشجویان
همچنین مشاهده کنید
نمایندگی زیمنس ایران فروش PLC S71200/300/400/1500 | درایو …
دریافت خدمات پرستاری در منزل
pameranian.com
پیچ و مهره پارس سهند
خرید میز و صندلی اداری
خرید بلیط هواپیما
گیت کنترل تردد
ایران اسرائیل دولت حجاب رئیس جمهور پاکستان گشت ارشاد رئیسی دولت سیزدهم کارگران رهبر انقلاب سریلانکا
سلامت کنکور عربستان سیل تهران هواشناسی سازمان سنجش فضای مجازی اصفهان شهرداری تهران پلیس زنان
تورم دلار خودرو قیمت خودرو قیمت دلار آفریقا قیمت طلا بازار خودرو سایپا بانک مرکزی ایران خودرو مسکن
خانواده تلویزیون مرگ ترانه علیدوستی فیلم سریال سینمای ایران موسیقی مهران مدیری
اینترنت کنکور ۱۴۰۳ عبدالرسول پورعباس
رژیم صهیونیستی غزه روسیه فلسطین جنگ غزه چین حماس طالبان ایالات متحده آمریکا اوکراین ترکیه طوفان الاقصی
پرسپولیس فوتبال جام حذفی آلومینیوم اراک استقلال فوتسال بازی بارسلونا تراکتور باشگاه پرسپولیس تیم ملی فوتسال ایران باشگاه استقلال
هوش مصنوعی سامسونگ ناسا الماس فیلترینگ ماه نخبگان
سازمان غذا و دارو مالاریا کاهش وزن سلامت روان آلزایمر زوال عقل